
Enzimas
Definición
Las enzimas son proteínas especiales que actúan como biocatalizadores en los organismos vivos. Su función principal es acelerar reacciones químicas que, de otra manera, serían muy lentas o no ocurrirían a temperatura y presión normales. Sin enzimas, la vida tal como la conocemos no sería posible.
Características principales
-
Especificidad: Cada enzima actúa sobre un sustrato concreto, que es la molécula sobre la que realiza su acción.
-
Reutilizables: No se consumen durante la reacción; pueden participar en muchas reacciones.
-
Sensibles al entorno: Su actividad depende de factores como temperatura, pH y concentración de sustrato.
-
Regulación: Pueden ser activadas o inhibidas por otras moléculas para controlar la velocidad de las reacciones.
Partes de una enzima
-
Sustrato: molécula que se transforma durante la reacción.
-
Centro activo: región de la enzima donde se une el sustrato y ocurre la reacción química.
Tipos de reacciones catalizadas
Las enzimas pueden intervenir en distintas reacciones del metabolismo, como:
-
Digestión de alimentos (amilasa, lipasa, proteasa).
-
Síntesis de moléculas biológicas (ADN polimerasa, ARN polimerasa).
-
Transformaciones metabólicas internas (glucógeno sintasa, hexoquinasa).
Ejemplos de enzimas importantes
-
Amilasa: convierte el almidón en azúcares simples.
-
Lipasa: transforma las grasas en ácidos grasos y glicerol.
-
Proteasa: rompe las proteínas en aminoácidos.
-
ADN polimerasa: sintetiza ADN durante la replicación celular.
-
Catalasa: descompone el peróxido de hidrógeno en agua y oxígeno.
Propiedades especiales
-
Catalizadores biológicos: aceleran reacciones sin consumirse.
-
Altamente específicas: solo reconocen ciertos sustratos.
-
Regulables: su actividad puede aumentar o disminuir según las necesidades de la célula.
-
Sensibles a condiciones externas: calor extremo o cambios de pH pueden desnaturalizarlas, haciendo que pierdan su forma y función.
Importancia biológica
-
Permiten que el metabolismo celular ocurra a velocidad suficiente para la vida.
-
Participan en la digestión, la síntesis de biomoléculas, la energía celular y la regulación metabólica.
-
Son esenciales para procesos vitales como la replicación del ADN, la contracción muscular, la defensa del organismo y la comunicación hormonal.
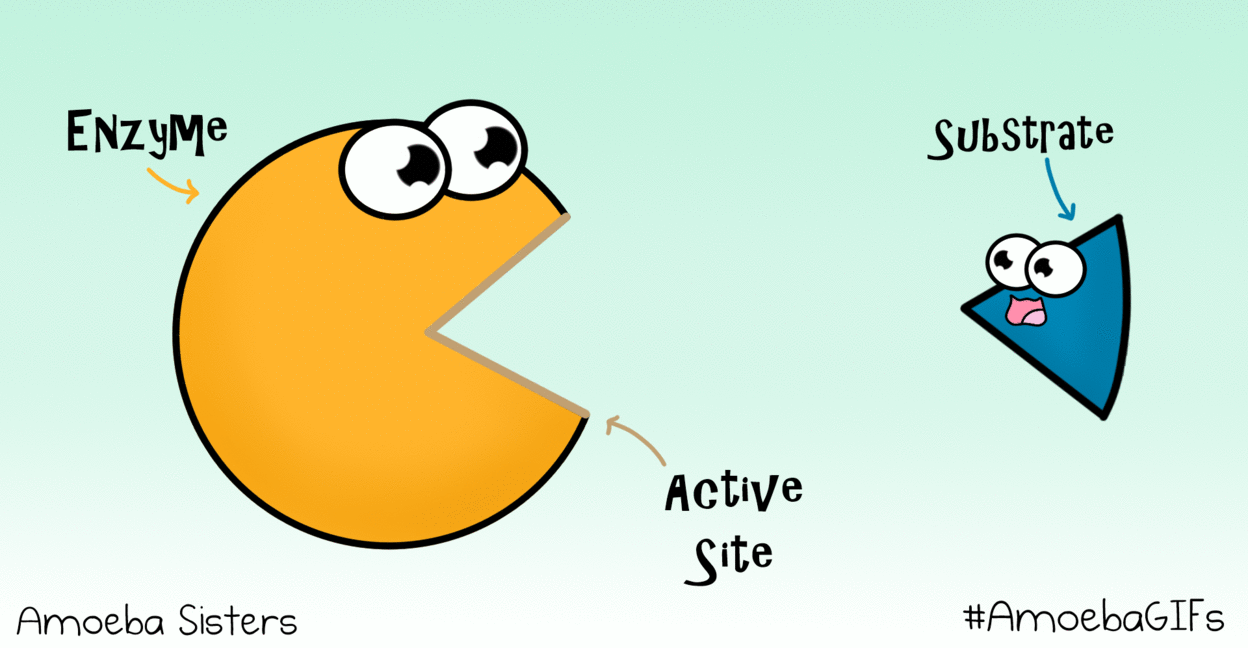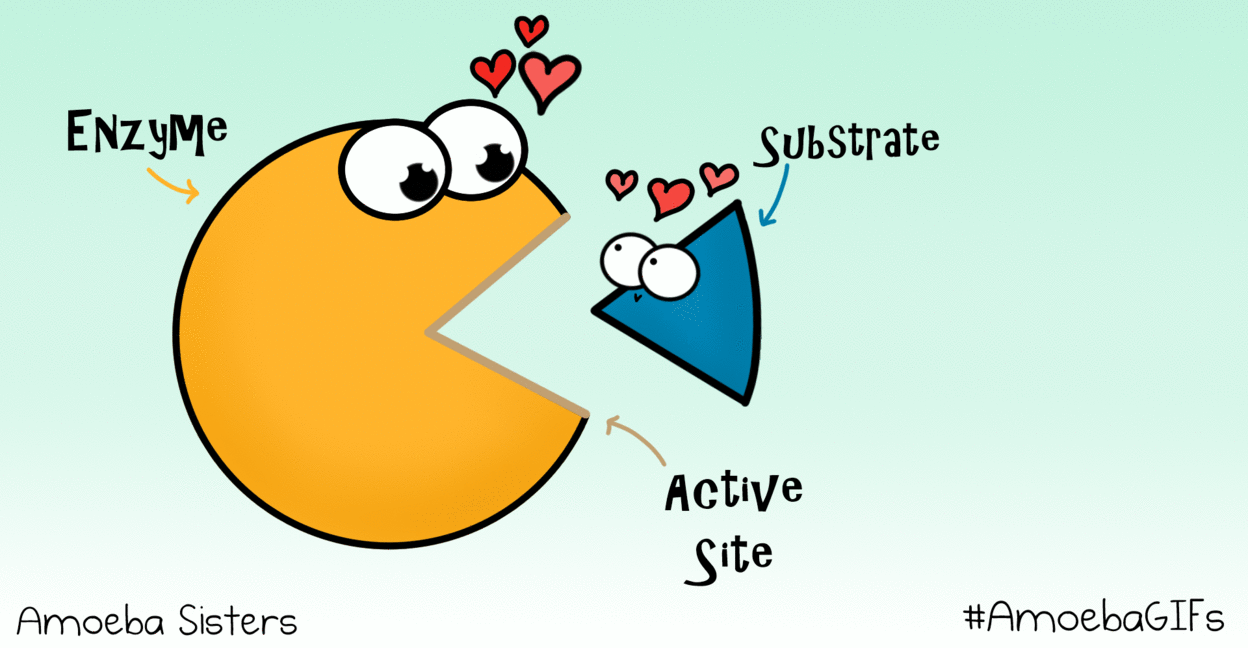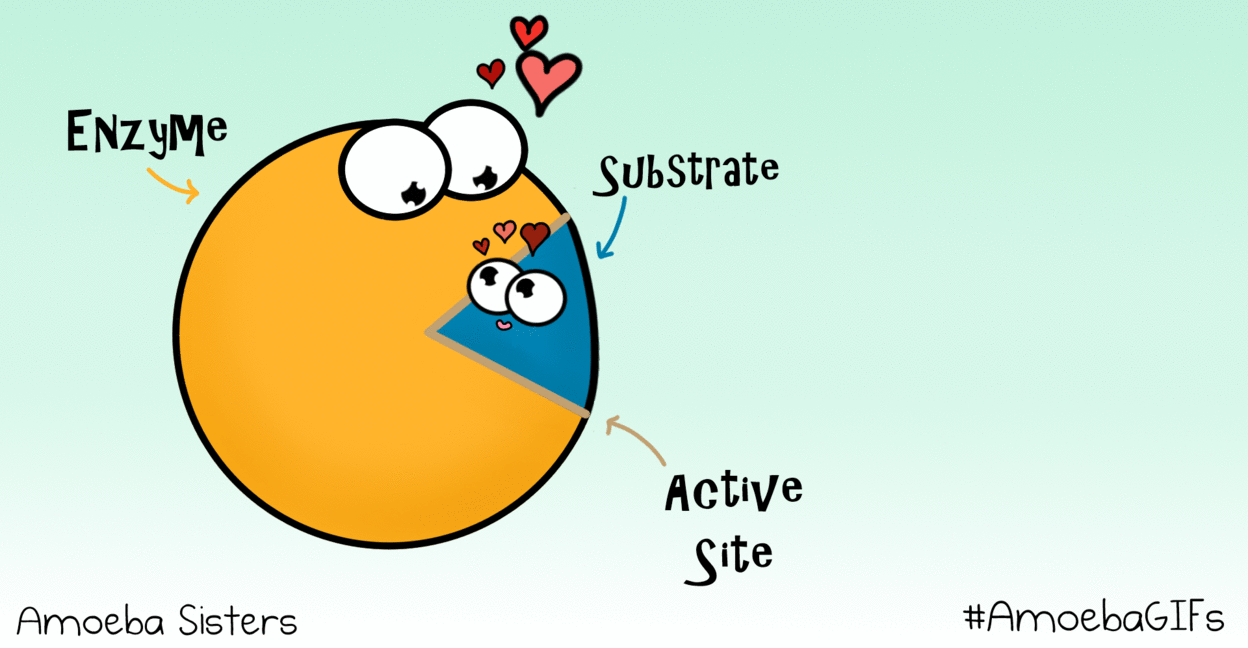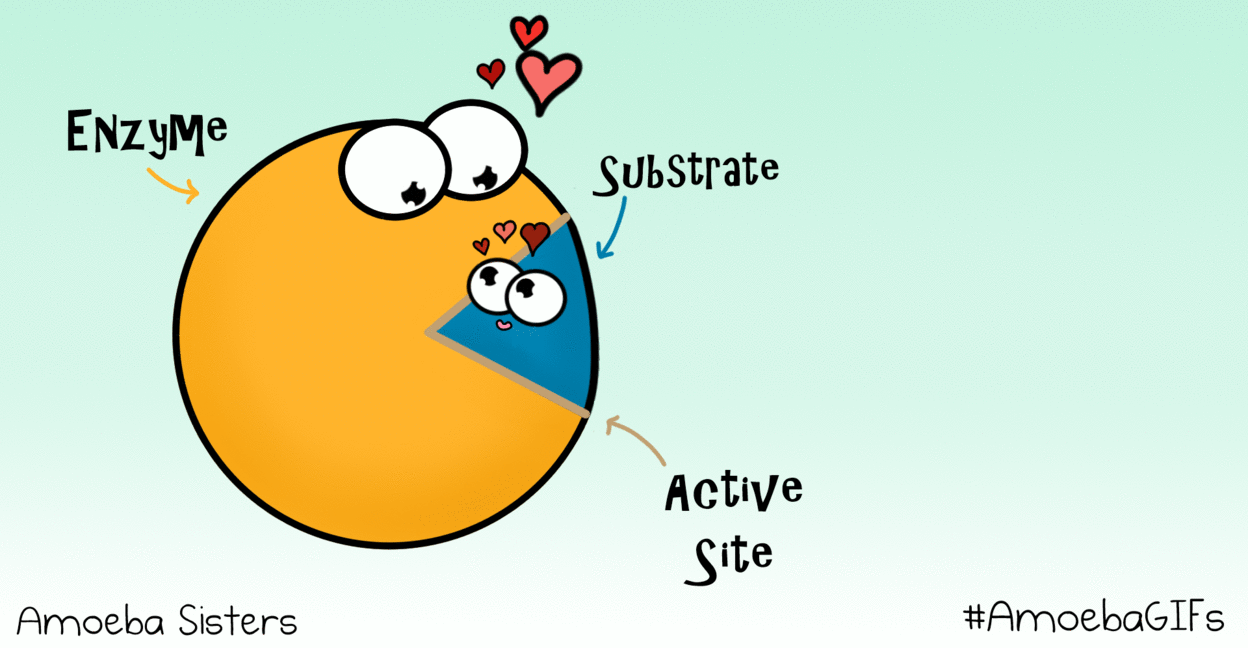


Estructura y sitio activo
-
Como todas las proteínas, están formadas por cadenas polipeptídicas.
-
Su conformación tridimensional genera invaginaciones donde se encuentra el sitio activo, el lugar donde se une el sustrato (la molécula sobre la que actúa la enzima).
-
La unión del sustrato puede producir un cambio temporal en la enzima, favoreciendo la reacción.
-
La especificidad: algunas enzimas actúan sobre un solo sustrato, mientras que otras pueden actuar sobre varios sustratos similares.
Nomenclatura
-
Las enzimas suelen recibir nombres según el sustrato o la reacción que catalizan:
-
ATP sintasa: síntesis de ATP.
-
Malato deshidrogenasa: reacción de oxidación-reducción del malato.
-
Tipos de enzimas
-
Oxidoreductasas: catalizan reacciones de oxidación-reducción.
-
Transferasas: catalizan la transferencia de grupos químicos.
-
Hidrolasas: rompen enlaces mediante incorporación de agua.
-
Liasas: rompen enlaces sin usar agua.
-
Isomerasas: catalizan la transformación de moléculas en sus isómeros.
-
Ligasas: unen moléculas entre sí.
Mecanismo de acción
-
Formación del complejo enzima-sustrato (ES): el sustrato se une al sitio activo mediante enlaces débiles, orientado de forma óptima para la reacción.
-
Modificación del sustrato: la enzima facilita la ruptura o formación de enlaces para generar el producto.
-
Formación y disociación del complejo enzima-producto (EP): el producto se libera y la enzima queda libre para actuar sobre otro sustrato.
Cinética enzimática
-
La velocidad de reacción depende de la concentración de enzima y sustrato, así como de la temperatura, pH y presencia de inhibidores.
-
Relación con el sustrato:
-
Etapa A: velocidad aumenta linealmente con la concentración de sustrato.
-
Etapa B: aumento de velocidad disminuye.
-
Etapa C: enzima saturada; la velocidad alcanza el máximo.
-
Efecto de la temperatura
-
Aumenta la actividad hasta un valor óptimo.
-
Temperaturas muy altas (≥60 °C) desnaturalizan la enzima y disminuyen su actividad.
Inhibidores enzimáticos
-
Sustancias que disminuyen la actividad de las enzimas.
-
Competitivos: se unen al sitio activo y compiten con el sustrato.
-
No competitivos: se unen en otro sitio y alteran la función de la enzima sin competir con el sustrato.



Escanea y juega


Para ver el video


